Yarı İletken Fiziği Serisi Bölüm 1- Katıların Kristal Yapısı
Giriş
Yarı iletken fiziği serimizin ilk bölümünde, karmaşık denklemlere ve konseptlere dalmadan önce katıların kristal yapısını ele alarak başlayacağız. Yarı iletkenlerin karakteristiğini, elektronik özelliklerini kavrayabilmemiz için atomların dizilişlerini anlamak büyük önem taşır. Bu giriş bölümü; yarı iletken malzemelerin ve aygıtların elektriksel karakteristiklerini belirleyen tek kristal yapıları ile kristal büyüme tekniklerine dair temel kuramsal çerçeveyi sunmaktadır. İşe önce çok kısa bir şekilde yarı iletken malzemeleri sınıflandırmakla başlayalım.
Yarıiletken Malzemeler
Yarı iletken malzemeler, iletkenlikleri metal ve yalıtkanların arasında olan malzemelerdir. Yarı iletken malzemeleri elemental (tek elementli) ve bileşik yarı iletkenler olarak sınıflandırabiliriz. Elemental yarı iletkenler periyodik tablodaki Grup IV elementleri arasındadır, bileşik yarı iletkenler ise Grup III ile Grup V veya Grup II ile Grup VI elementlerinin bazı özel kombinasyonlarından oluşur.

Figürde gösterilenlerin dışında, üç elementli bileşik yarı iletkenler de oluşturabiliriz, örneğin:
Malzeme özelliklerinin seçiminde esneklik sağlayan daha karmaşık yarı iletkenler de oluşturulabilir.
Katı Türleri
Katıları genel yapı itibariyle üç tür ile sınıflandırabiliriz: Amorf katılar, çoklu (poli) kristal katılar ve tek (mono) kristal katılar. Amorf katıların atomları düzenli ve periyodik bir kafes yapısı oluşturmaz. Uzun menzilli düzen yoktur. Çoklu kritstal katılar birçok küçük kristal tanesinden (grain) oluşur. Her tane kendi içinde düzenlidir ama yönleri farklıdır. Tek kristal katılarda tüm yapı boyunca atomlar tek ve kesintisiz bir kristal kafes düzeni oluşturur. Bir başka ifadeyle bu tek kristalli malzemeler, ideal durumda, tüm hacimleri boyunca yüksek derecede düzenli ve geometrik olarak periyodik bir atom dizilimine sahiptir.
Tek kristalli yapının en önemli avantajı, tane sınırlarının bulunmamasıdır. Çünkü tane sınırları elektriksel özellikleri olumsuz etkileyebilir. Bu nedenle tek kristalli malzemelerin elektriksel özellikleri, tek kristalli olmayan (örneğin polikristal) malzemelere göre genellikle daha üstündür. Aşağıdaki figürde bu üç türdeki katıların iki boyutlu temsilleri verilmiştir.

Kafes Geometrisi (Space Lattices)
Kristal yapıyı matematiksel olarak tanımlamak için iki kavramın birleşimi anlatılır:
Örgü (Lattice): Grup teorisi dilinde bir örgü (lattice), -boyutlu Öklid uzayı grubunun ayrık bir alt grubu (discrete subgroup), bu uzaydaki bir sonsuz noktalar kümesidir. Aşağıda belirtilen özelliklere sahiptir:
- Örgüdeki iki noktanın koordinat bazında toplanması veya çıkarılması, başka bir örgü noktası verir.
- Örgü noktalarının hepsi belli bir minimum mesafe ile ayrılmıştır.
- Örgüdeki herhangi bir noktanın çevresi, örgüdeki herhangi başka bir noktanın çevresi ile eş değerdir.

Temel (Basis): Kristal yapıyı göz önünde bulundurursak, örgüdeki tekrar eden atom grubudur.
İlkel ve Birim Hücre
Birim Hücre: Periyodik yapının tekrar eden temel yapı taşlarıdır. Tek kristalli katı yapısında üç boyutlu örgü, tekrarlayan (periyodik) atom gruplarından oluştuğundan, tüm örgü yerine sadece tekrarlayan temel birim hücreyi ele alabiliriz.
İlkel Birim Hücre: Tam olarak tek bir örgü noktası içeren birim hücredir.
Periyodik herhangi bir yapı, tekrar eden bir motif örgüsü ile ifade edilebilir. İki ve üç boyutlu örgüdeki ilkel örgü vektörü seçimi tek (unique) değildir. Seçebileceğimiz sonsuz sayıda ilkel örgü vektörü vardır. Bazen, üzerinde çalışmayı daha basit hale getirmek için ilkel (primitive) olmayan bir birim hücre tanımlamak yararlı olabilir. Buna geleneksel (conventional) birim hücre denir. Neredeyse her zaman bu geleneksel birim hücreler, eksenleri birbirine dik (ortogonal) olacak şekilde seçilir.
Aşağıdaki görseldeki vektör gösterimlerini (iki boyut için)
şeklinde yazabiliriz.

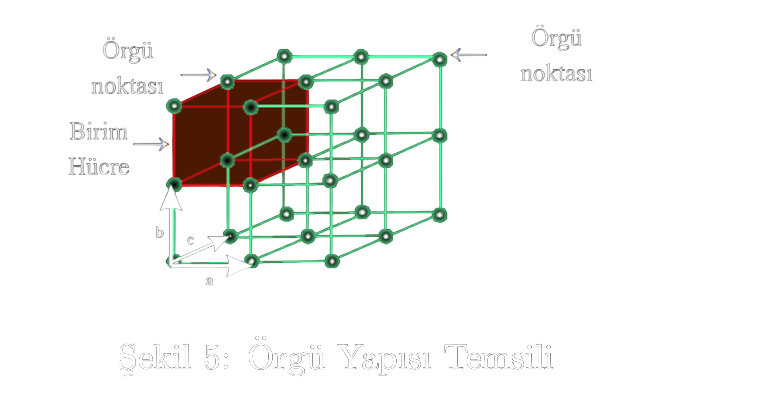
Genelleştirilmiş bir üç boyutlu örgü yapısını ve birim hücreyi şekil 5'te görebiliriz. Bu birim hücre ve örgü arasındaki ilişkiyi vektörlerle karakterize ederiz. Orijinin konumu isteğe bağlı olduğundan basitlik için x,y,z'ye pozitif sayılar diyebiliriz.
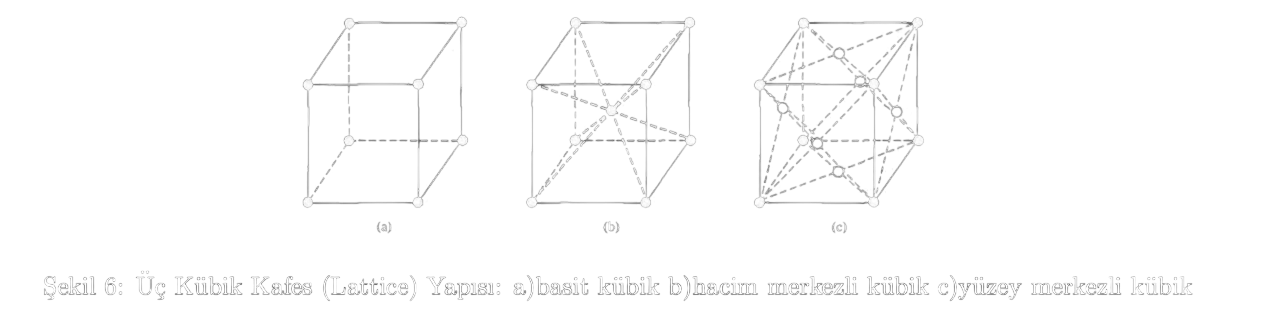
Basit Kristal Yapılar
Yarı iletken kristallerini tartışmadan önce, basit kristal yapılarını ve bu yapıların özelliklerini ele alalım. Basit kübik yapıda küpün her köşesinde birer atom bulunur. Hacim merkezli küpte ek olarak kübün merkezinde bir atom daha bulunur; yüzey merkezli kübik yapıda ise köşedeki atomlar haricinde kübün her yüzeyinin merkezinde birer atom bulunur.
Birim hücredeki kafes noktalarının sayımıyla ilgili bir hatırlatma:
Çoğu durumda, kafes noktaları hücrenin köşelerinde ya da kenarlarında bulunan birim hücreleri kullanırız.
Eğer bir kafes noktası hücrenin sınırında yer alıyorsa, hücre içinde kalan kısmı kadar, yani içerideki payına göre, bu noktanın kesirli olarak sayılması gerekir. Hacim merkezli kübik kafesten örnek vermek gerekirse, bu kafesin birim hücresinde her bir köşede 8 örgü noktası bulunur, geleneksel birim hücrede bu noktaların 'i yer alır, hacim merkezindeki noktanın ise tamamını kapsar; yani geleneksel hücre içerisinde toplam
örgü noktası yer alır. Kübik olmayan diğer kafes yapılarını şu an burada detaylandırmayacağız.
Kristal Düzlemleri Ve Miller İndisleri (Miller Indices)
Gerçek kristaller sonlu olduğundan nihayetinde belli bir yerde son bulur. Yarı iletken cihazlar bir yüzeyde veya yüzeye yakın bir yerde üretilir, bu nedenle yüzey özellikleri cihaz özelliklerini etkileyebilir. Bu, yarıiletken üretimi (wafer kesimi) için çok kritiktir. Miller indisleri, kristal içindeki düzlemleri ve yönleri tanımlamak için kullanılan bir gösterim sistemidir. Miller indeksleri olan üç tam sayı (hkl) şeklinde yazılır ve bu sayılar özetle düzlemin x,y,z eksenlerini kestiği noktaların çarpmaya göre tersinin (reciprocal) tam sayı haline getirilmesi ile elde edilir. Yani Miller indisleri aslında "ters örgü vektörlerinin" bileşenleridir. Yani indisli bir düzlem, ters örgüdeki
vektörüne diktir. Neden direkt kesim noktalarını değil de terslerini alıyoruz? Bunun sebepleri; sonsuz değerlerden kurtulmak, kristalin periyodikliğini temsil etmek ve kırınım deneyleriyle uyum (X-ışını kırınımı bize doğrudan ters örgüyü gösterir). Bir düzlem bir eksene paralelse, o ekseni teorik olarak "sonsuzda" keser. Tersini alarak sonsuzları sıfıra dönüştürüyor, tüm paralel düzlemleri tek bir "aile" adı altında topluyor ve deneysel verilerle teoriyi aynı matematiksel dilde buluşturuyoruz. , ve düzlemleri yarı iletken teknolojisinde en sık kullanılan düzlemlerdir.

Elmas Yapısı
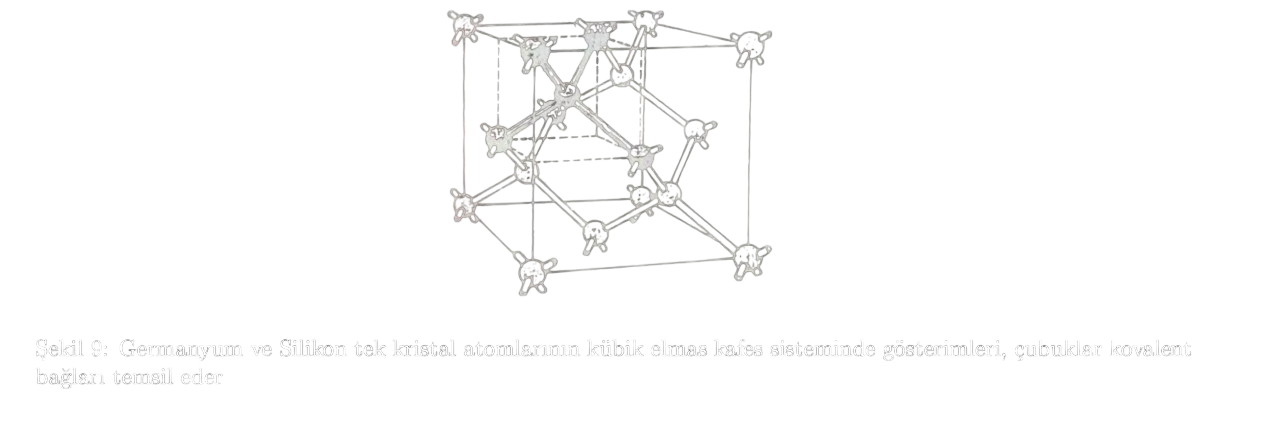
En yaygın elemental yarı iletken materyali olan silikon, bir grup IV elementidir ve elmas kristal yapısına sahiptir. Germanyum da aynı şekilde bir grup IV elementi ve elmas yapısındadır. Elmas yapının birim hücresi şimdiye kadar değindiğimiz basit kübik yapıdan biraz daha karmaşıktır. Tetrahedral (dört yüzlü) yapıdaki her atomun dört en yakın komşusu vardır ve bu yapı, elmas kafesinin temel yapı taşıdır. Diğer bir deyişle elmas kübik kafes, bu tekrar eden her bir ilkel hücrede tetrahedral bağlarla bağlanmış atomlardan meydana gelir; bu atomlar hücrenin her bir boyutunda hücre genişliğinin 1/4’ü kadar bir uzaklıkla birbirinden ayrılmıştır.
Elmas kafesi, birbirini kesen iki yüzey merkezli kübik (FCC) kafesin birleşimi olarak da düşünülebilir; bu iki kafes, her bir boyutta birim hücre genişliğinin 1/4’ü kadar ötelenmiştir.

Atomik Bağlar
Bizler burada çeşitli tek kristal yapılarını inceliyoruz. Bu noktada şu soru ortaya çıkar: Belirli bir atom topluluğu için neden bir kristal yapı diğerine tercih edilir? Doğanın temel yasalarından biri, termal dengedeki bir sistemin toplam enerjisinin mümkün olan en düşük değere yönelmesidir. Atomların bir araya gelerek katı bir yapı oluşturması ve toplam enerjiyi en aza indirmesi sürecindeki etkileşim, ilgili atom ya da atomların türüne bağlıdır. Bu nedenle kristal içindeki atomlar arasındaki bağın ya da etkileşimin niteliği, o kristali oluşturan atomların özelliklerine göre belirlenir. Atomlar arasında güçlü bir bağ bulunmazsa, katı bir yapı oluşturacak şekilde bir arada kalamazlar. Atomların arasındaki etkileşimler kuantum mekaniğiyle açıklanır ancak bunu detaylandırmayı sonraki bölümlere bırakıyoruz. Yarıiletkenlerin enerji bantları ve elektriksel iletkenliği, bu atomların periyodik diziliminden ve kurdukları kovalent bağlardan doğar.
Kristal Kusurları ve Safsızlıklar (Imperfections and Impurities)
Her ne kadar ideal bir kristalin kusursuz bir periyodik yapısını düşünsek de, gerçekte kristallerde periyodiklik kusurlarla bozulur. Bu durum, elimizdeki yarı iletken malzemenin elektriksel özelliğini doğrudan etkiler; hatta bazen malzemenin elektriksel özellikleri tamamen kontrollü kusurlar oluşturarak belirlenebilir. Buna serinin daha sonraki bölümlerinde "doping" anlatırken değineceğiz.
-
Termal Titreşimler (Lattice Vibrations): Tüm kristallerde ortak olan tek kusurdur. Mutlak sıfır () üzerindeki her sıcaklıkta atomlar denge noktaları etrafında rastgele titreşirler. Bu durum: Atomlar arası mesafenin sürekli dalgalanmasına neden olur. Mükemmel geometrik düzeni anlık olarak bozar. Yarı iletkenlerde yük taşıyıcılarının saçılmasına (scattering) neden olarak direnci etkiler.
-
Noktasal Kusurlar (Point Defects):
Tek bir atomu veya atom bölgesini ilgilendiren kusurlardır:
Boşluk (Vacancy): Kristal örgüsündeki bir atomun yerinde olmaması durumudur.
Ara Yer Atomu (Interstitial): Bir atomun, normal örgü sahalarının arasındaki boşluklara yerleşmesidir.
Frenkel Kusuru: Bir boşluk ve bir ara yer atomunun birbirine yakın olup etkileşime girmesiyle oluşur.
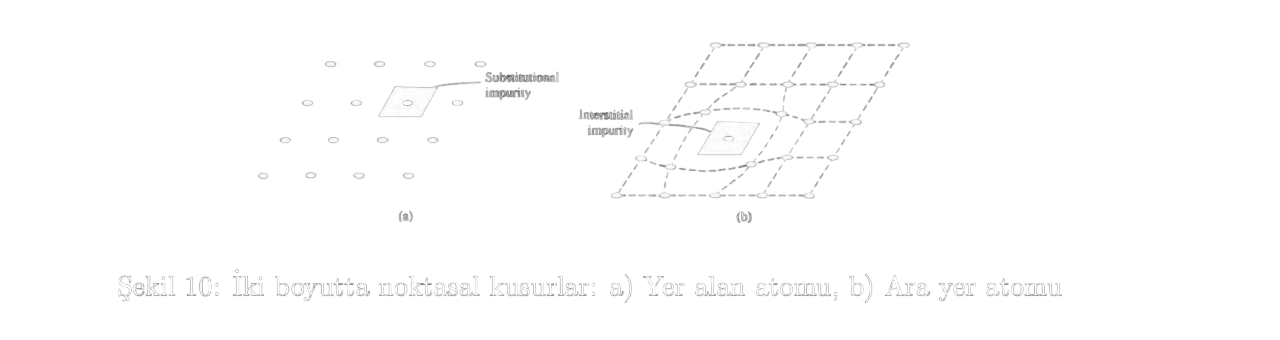
- Çizgisel Kusurlar (Line Defects):
Atomların bir sıra boyunca eksik olması veya yanlış dizilmesiyle oluşur:
Kenar Dislokasyonu (Line Dislocation): Kristal yapısına fazladan bir atom düzleminin girmesi veya bir sıranın tamamen eksik olmasıdır. Dislokasyonlar kristal büyümesinde yapıcı bir rol oynayabilir.

Bu kusurlar hem geometrik periyodikliği hem de ideal kimyasal bağları bozar, elektriksel özellikleri tahmin edilmesi güç bir biçimde değiştirir.
Yarı iletken malzemelerin büyütülmesi ve büyütme teknikleri konusuna ileride değineceğiz. Sıradaki yazımız olacak Bölüm 2'de, bu malzemelerin özelliklerini anlamamız için gerekli olan kuantum mekaniği temelleri ve katıların kuantum teorisi olarak iki ana başlığı anlatacağız. Kemerlerinizi bağlayın.
Kaynakça
- Semiconductor Physics And Devices by Donald A. Neamen Third Edition
- The Oxford Solid State Basics by Steven H. Simon
- https://en.wikipedia.org/wiki/Lattice_%28group%29
- https://www.careers360.com/chemistry/crystal-lattices-and-unit-cells-topic-pge
- https://en.wikipedia.org/wiki/Diamond_cubic
- https://www.researchgate.net/figure/Miller-indices-indicating-the-plane-perpendicular-to-the-vector-given-for-the-cubic_fig7_302838100